L’ occhio come tutti gli altri organi ha una circolazione sanguigna. Il sangue passa dai vasi arteriosi al letto capillare per essere drenato nei vasi venosi e defluire verso la vena centrale della retina.
Quando si verifica un’ occlusione a livello di un vaso venoso si manifestano tutta una serie di conseguenze a livello oculare che vanno strettamente tenute sotto controllo e sottoposte a terapia, perchè possono determinare un calo del visus, a volte anche significativo.
Quando si occlude la vena centrale della retina, cioè quella a cui affluiscono tutte le altre diramazioni venose, si formano emorragie su tutta la superficie retinica e il calo visivo può essere più severo. Tuttavia con la creazione di circoli collaterali di compenso efficienti la situazione può migliorare nel tempo.
Quando si verifica un’ occlusione venosa della branca superiore o inferiore della vena centrale della retina, si parla di occlusione emiretinica, più rara dell’ occlusione della vena centrale retinica.
Invece la forma più frequentemente riscontrabile nella pratica clinica per l’oculista è rappresentata dall’ occlusione venosa di branca, che coinvolge solo una delle diramazioni venose secondarie (le occlusioni venose di branca sono tre volte più frequenti di quelle della vena centrale della retina).
EPIDEMIOLOGIA
Le occlusioni venose di branca costituiscono la patologia retinica vascolare più diffusa dopo la retinopatia diabetica e rappresentano una comune causa di calo visivo nella popolazione di età avanzata.
Hanno un’ incidenza compresa tra lo 0,5 e l’1,2%. La prevalenza è maggiore tra i 60 e i 70 anni.
EZIOPATOGENESI E DECORSO CLINICO
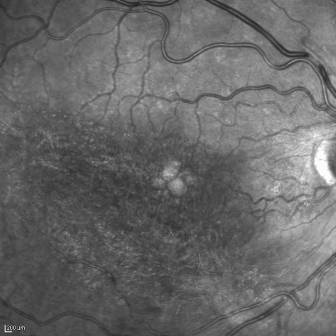
Il tipico aspetto alla lampada a fessura del fondo dell’ occhio nell’ occlusione venosa di branca è caratterizzato dalla presenza di emorragie retiniche superficiali e profonde, più o meno numerose secondo la gravità dell’ occlusione, distribuite seguendo il decorso della vena interessata dall’ occlusione.
Fattori di rischio sono l’età avanzata, oltre i 65 anni, l’ ipertensione arteriosa sistemica presente nel 64% dei pazienti di età superiore ai 50 anni, i disturbi vascolari periferici, il diabete mellito presente nel 10% dei pazienti di età superiore ai 50 anni, l’ ipercolesterolemia, l’ aumento della pressione intraoculare, le patologie cardiovascolari, etc (meno frequentemente patologie concomitanti quali la sarcoidosi oculare,la sindrome di Behçet, la malattia di Eales, la malattia di Coats, l’emangioma vascolare retinico, stati di ipercoagulabilità congeniti o acquisiti, etc.
L’ insorgenza di questa patologia è correlata alla presenza degli incroci artero-venosi.
L’ occlusione venosa di branca infatti si riscontra più frequentemente nella metà temporale della retina, per la presenza a questo livello di un maggior numero di incroci artero-venosi.
Un’ arteriola con la parete ispessita a causa dell’ arteriosclerosi può esercitare una compressione meccanica sulla venula sottostante a livello di un incrocio artero-venoso, determinando una riduzione del diametro del lume venoso e la comparsa di una dilatazione a monte.
Il restringimento vasale comporta un aumento della velocità del flusso del sangue nel punto ove viene esecitata la compressione, e quindi la formazione di turbolenze a valle dell’ icrocio artero-venoso, che provocano perdita della regolarità del fisiologico flusso sanguigno.
Nel flusso sanguigno normalmente le piastrine occupano la parte centrale del fluido che passa, e sono separate dalla parete del vaso dal plasma, una parte più fluida. Se si instaurano delle turbolenze le piastrine vengono a contatto con la parete vasale, e si attiva l’ emostasi. Il danno alla parete dei vasi porta alla formazione di un trombo. Si possono creare più o meno rapidamente circoli collaterali di compenso nell’ area dell’ occlusione.
Col tempo (dopo circa 3 settimane dall’ evento occlusivo) il trombo si organizza, si ha una ricanalizzazione del vaso, i vasi collaterali formati diventano strutturalmente maturi.
Le BRVO si suddividono in:
-forme non ischemiche
-forme ischemiche
Le forme non ischemiche sono circa 1/3, ed hanno una prognosi migliore, con maggiore recupero della vista.
Le forme ischemiche sono 2/3, hanno prognosi peggiore per quel che concerne il recupero visivo e possono essere complicate, nel 20% dei casi, da formazione di neovasi ( le complicanze saranno tanto più gravi quanto maggiore sarà l’estensione dell’area di retina ischemica , cioè non più adeguatamente perfusa).
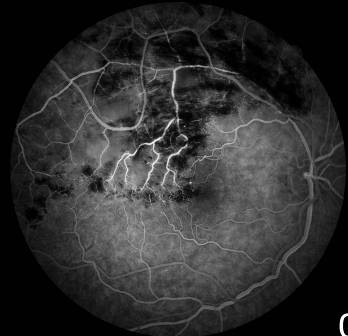
La fluorangiografia è una metodica diagnostica strumentale che consente tramite un’ iniezione nella vena del braccio di un colorante giallo, la fluoresceina sodica, lo studio dinamico della circolazione retinica.
Dà informazioni generali sulla circolazione retinica, quali tortuosità e irregolarità di calibro dei vasi, grado di compressione a livello degli incroci artero-venosi, e permette di individuare il sito dell’ occlusione, in cui si evidenzia perdita di colorante, di delimitare l’area retinica interessata, ed evidenziare la presenza di eventuali circoli di compenso.
Differenzia forme occlusive ischemiche e forme non ischemiche.
Tramite un altro esame strumentale, l’ OCT, si può evidenziare l’ eventuale presenza di edema maculare.
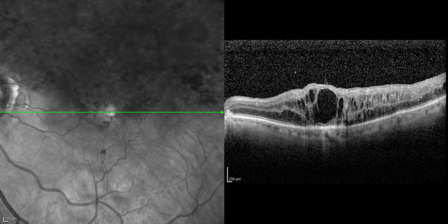
Alcune forme di occlusione venosa di branca sono caratterizzate da comparsa di edema maculare (ovvero fluido all’ interno della parte centrale della retina) responsabile, quando presente, di un’importante compromissione della funzione visiva. Quando si ha edema aumenta lo spessore della parte centrale della retina. Col tempo l’ edema può diventare cronico.
Alla FAG spesso si evidenzia con un aspetto caratteristico definito a “petalo di fiore”.
All’ OCT un’ imbibizione diffusa della retina si manifesta con un caratteristico aspetto spugnoso.
L’ edema retinico costituisce una complicanza piuttosto frequente.
Più gravi e rare complicanze possono essere un sanguinamento nel vitreo (emovitreo) e il distacco di retina.
TERAPIA DELLE OCCLUSIONI VENOSE DI BRANCA
In primo luogo bisogna indagare, individuare e trattare gli eventuali fattori di rischio.
L’ ischemia retinica, ovvero una non perfusione retinica con ampia estensione, sta ad indicare un’ alta probabilità che si sviluppi una complicanza (come la formazione di neovasi)
Il trattamento argon laser è efficace nel prevenire la formazione di neovasi e l’ eventuale sanguinamento nel vitreo.
Il triamcinolone somministrato con iniezione intravitreale riduce l’ edema maculare .
Nel 2009 la FDA ha approvato per il trattamento dell’ edema maculare conseguente ad occlusioni venose un dispositivo intravitreale biodegradabile a lento rilascio di desametasone.
L’ emivita intravitreale del desametasone è breve, di 5,5 ore. Per prolungare il suo effetto, è stato associato ad altri componenti (un copolimero che contiene acido lattico ed acido glicolico).
Il picco massimo di concentrazione del desametasone nel vitreo è stato riscontrato dopo 2 mesi, e concentrazioni ancora efficaci sono state rilevate fino a 6 mesi dall’ iniezione.
L’ applicatore sterile, monouso, crea un accesso auto chiudente.
Il trattamento precoce dell’ edema maculare con desametasone consente di ottenere migliori risultati funzionali.
Sul piano della sicurezza il temuto effetto collaterale dell’ aumento della pressione dell’ occhio può essere prevedibile, ed è comunque controllabile con la somministrazione di colliri antiglaucomatosi.
Il VEGF stimola la proliferazione delle cellule endoteliali vasale e induce la permeabilità vascolare. I livelli vitreali di VEGF sono elevati nell’ edema maculare conseguente a BRVO e sono correlati alla sua severità.
La terapia con anti- VEGF quali il ranibizumab (Lucentis,Genentech, Inc., USA) e il bevacizumab (Avastin, Genentech,Inc., USA) può essere presa in considerazione come trattamento esclusivo o in associazione all’ impianto di desametasone.
Il Ranibizumab è un frammento di immunoglobulina umanizzata ricombinante che lega e inibisce l’ attività biologica di tutte le isoforme di VEGF-A umano. E’ stato approvato dalla FDA per il trattamento della AMD neovascolare,dell’edema maculare nelle occlusioni venose retiniche e dal 2012, per l’edema maculare diabetico.
Il Bevacizumab è un intero anticorpo monoclonale ricombinante umanizzato IgG che inattiva tutte le isoforme di VEGF-A ed è approvato anche per l’ uso sistemico nel trattamento di certe forme di cancro metastatico